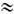 1) и слабых (a<<1) Э. Один и тот же Э. в разных растворителях может образовывать
растворы с разной a.
1) и слабых (a<<1) Э. Один и тот же Э. в разных растворителях может образовывать
растворы с разной a.Электролиты - жидкие и твёрдые вещества, обладающие ионной проводимостью, т. е. проводники, в к-рых
электрич. ток обусловлен движением ионов (проводники 2-го рода). Электрич;
ток в Э. сопровождается хим. реакциями на электродах(см. Электролиз ).В
нек-рых случаях наблюдается смешанная электропроводность - электронно-ионная
(напр., в растворах щелочных металлов в жидком NH3); высокой проводимостью
обладают Э. с протонной проводимостью.
К жидким Э. относятся расплавы
солей (ионные жидкости), водные и неводные растворы солей, оснований и кислот,
к-рые, в свою очередь, часто называют Э. К твёрдым Э. относятся ионные кристаллы
с дефектами кристаллич. структуры с низкой ионной проводимостью (до 10-10
Ом.см ). К ним относятся также кристаллич. вещества, в к-рых подструктура
отдельных ионов (в отличие от подструктуры остальных ионов) разупорядочена и
электропроводность к-рых высока (см. Ионные суперпроводники ).К твёрдым
Э. относится и особый класс высокомолекулярных соединений - полиэлектролиты.
В твёрдых Э. проводимость иногда может быть обусловлена движением ионов только
одного знака (униполярная проводимость); к таким Э. относятся, напр., AgCl -
в проводимости участвуют только ионы Ag+ , ВаСl2 - только
ионы Cl-.
Наиболее широко применяются
и хорошо изучены водные растворы Э. Они входят в состав живых организмов и участвуют
во всех жизненно важных процессах. Свойства растворов Э. определяются степенью
электролитич. диссоциации a, к-рая возрастает с ростом диэлектрич. проницаемости
растворителя e. Поэтому для получения растворов Э. обычно используют полярные
жидкости с высокой e (вода, спирт и др.). По степени диссоциации условно различают
растворы сильных (a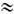 1) и слабых (a<<1) Э. Один и тот же Э. в разных растворителях может образовывать
растворы с разной a.
1) и слабых (a<<1) Э. Один и тот же Э. в разных растворителях может образовывать
растворы с разной a.
В полярных растворителях
в растворах Э. создаются т.н. с о л ь в а т н ы е с т р у к т у р ы - более
или менее устойчивые комплексы иона с ближайшими молекулами растворителя, обусловленные
межатомными взаимодействиями и межмолекулярными взаимодействиями. Между сольва-токомплексом и остальным раствором происходит непрерывный обмен
молекулами, частота к-рого определяется характером и прочностью связей (энергией
сольватации) в комплексе.
Электролитич. диссоциация
приводит к увеличению общего числа частиц в растворе, поэтому свойства разбавленных
растворов Э. отличаются от свойств обычных разбавленных растворов. Так,
происходит увеличение осмотич. давления раствора и отклонение от ур-ния Вант-Гоффа
(см. Осмос ),понижение давления пара растворителя над раствором и его
отклонение от Рауля закона ,возрастание температуры кипения и снижение температуры
замерзания раствора Э.
Весьма разбавленные растворы
слабых Э. по свойствам близки к идеальным растворам и описываются классич. теорией
электролитич. диссоциации. Свойства разбавленных растворов сильных Э. вследствие
межионных взаимодействий отличны от свойств идеальных растворов и описываются
теорией Дебая-Хюккеля. В рамках этой теории удовлетворительно объясняется концентрац.
зависимость коэффициентов активности ионов, осмотич. коэффициентов, электропроводности,
диффузии, вязкости, и др. При повышении концентрации сильных Э. необходимо учитывать
размеры ионов и влияние сольватации на межионные взаимодействия.
При росте концентрации
- в т.н. переходной области - структура раствора меняется, т. к. мн. молекулы
растворителя связаны с ионами Э. в сольватокомплексы. В области концентрированных
растворов их структура приближается к структуре соответствующих ионных расплавов
или даже кристаллов, что экспериментально подтверждено спектроскопическими и
нейтронографическими исследованиями.
К ионным проводникам, к-рыми
являются Э., применим Ома закон (для растворов Э.- за исключением областей
сильных электрич. полей и высоких частот). Удельная электропроводность у Э.
значительно ниже, чем у электронных проводников (обычно от 1 до 10-10
Ом.см-1).
В растворах Э. для характеристики
проводимости пользуются также параметром молярной электропроводности
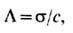
где s - уд. электропроводность
раствора, с-мол. концентрация раствора. В разбавленных растворах
сильных Э. а пропорциональна с, т. е. L практически постоянна. В более
концентрированных растворах сильных Э. L падает из-за роста межионных взаимодействий;
зависимость L от концентрации описывается ур-нием Онсагера:
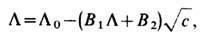
где B1
и В2 - функции температуры вязкости и диэлектрич. проницаемости
растворителя. В растворах слабых электролитов L падает с ростом с уже
в разбавленных растворах из-за уменьшения степени диссоциации Э.
В электрич. полях большой напряжённости (св. 104- 105 В/см) и в полях высокой частоты L резко возрастает, т. к. в этих случаях межионные и межмолекулярные взаимодействия значительно уменьшаются вследствие увеличения скорости ионов (см. также Химическая термодинамика).

Релятивисты и позитивисты утверждают, что "мысленный эксперимент" весьма полезный интрумент для проверки теорий (также возникающих в нашем уме) на непротиворечивость. В этом они обманывают людей, так как любая проверка может осуществляться только независимым от объекта проверки источником. Сам заявитель гипотезы не может быть проверкой своего же заявления, так как причина самого этого заявления есть отсутствие видимых для заявителя противоречий в заявлении.
Это мы видим на примере СТО и ОТО, превратившихся в своеобразный вид религии, управляющей наукой и общественным мнением. Никакое количество фактов, противоречащих им, не может преодолеть формулу Эйнштейна: "Если факт не соответствует теории - измените факт" (В другом варианте " - Факт не соответствует теории? - Тем хуже для факта").
Максимально, на что может претендовать "мысленный эксперимент" - это только на внутреннюю непротиворечивость гипотезы в рамках собственной, часто отнюдь не истинной логики заявителя. Соответсвие практике это не проверяет. Настоящая проверка может состояться только в действительном физическом эксперименте.
Эксперимент на то и эксперимент, что он есть не изощрение мысли, а проверка мысли. Непротиворечивая внутри себя мысль не может сама себя проверить. Это доказано Куртом Гёделем.
Понятие "мысленный эксперимент" придумано специально спекулянтами - релятивистами для шулерской подмены реальной проверки мысли на практике (эксперимента) своим "честным словом". Подробнее читайте в FAQ по эфирной физике.
|
|